הקשר המפתיע: כיצד היסטמין עשוי לגרום לטיקים ותסמינים נוספים?
הקשר המפתיע בין היסטמין וטיקים חושף כי המולקולה המוכרת לנו מעולם האלרגיות היא למעשה מוליך עצבי מעורר רב-עוצמה במערכת העצבים המרכזית. בילדים עם רגישות ביולוגית, עודף היסטמין הנובע מחיידקי מעיים, תאי מאסט או תהליכים דלקתיים, עלול להחמיר טיקים, חרדה, OCD ותסמיני ADHD. המאמר שלפניכם בוחן את השרשרת הביולוגית השלמה – מהמיקרוביום ועד לתפקוד המוח – ומציע גישה טיפולית מתקדמת.
נקודות מפתח למאמר
- היסטמין תפקיד כפול: מתווך דלקתי ומוליך עצבי מעורר, העשוי להחמיר טיקים, חרדה, OCD ו‑ADHD.
- מקורות: חיידקי מעיים, תולעים ואלרגנים סביבתיים המשחררים היסטמין מתאים חיסוניים.
- פירוק היסטמין תלוי בין היתר באנזימי DAO/HNMT.
- טיפול יעיל משלב מנגנונים ביולוגיים המושפעים מהיסטמין, מייצבי מאסט ותזונה דלת היסטמין.
מילות פתיחה
כשאנחנו חושבים על היסטמין, רובנו מדמיינים מיד התעטשויות, נזלת ועיניים דומעות, חלק מתסמיני האלרגיה הקלאסיים של עונת המעבר. זוהי התמונה המוכרת, אך היא מספרת רק חלק קטן מהסיפור. היסטמין הוא הרבה יותר מסתם מולקולה שגורמת לנו להצטייד בטישו. למעשה, הוא ממלא תפקיד עוצמתי ופחות מוכר במוח שלנו כמוליך עצבי מעורר (neuro-stimulatory neurotransmitter) שעשוי להניע תסמינים נוירולוגיים והתנהגותיים אצל ילדים, ביניהם חרדה, OCD וטיקים.
במאמר זה נצלול לעומק ונחשוף תובנות מפתיעות לגבי המקורות האמיתיים של עודף היסטמין בגוף, נבחן את המנגנונים הביולוגיים שמאחורי הקשר הזה, ונראה כיצד ניתן לנהל אותו בצורה חכמה ויעילה יותר מאשר רק הימנעות ממזונות מסוימים. נתבסס על מחקרים עדכניים שמצביעים על קשר ישיר בין עודף היסטמין לבין תסמינים נוירו-פסיכיאטריים אצל ילדים, כולל אלו שסובלים מ-PANS/PANDAS.
הקשר הביולוגי בין היסטמין לטיקים ותסמינים נוירולוגים נוספים
להיסטמין יש תפקיד כפול ומשמעותי: הוא גם מתווך דלקתי (pro-inflammatory mediator) שמגביר תגובות חיסוניות, וגם מוליך עצבי מעורר שמשפיע ישירות על פעילות המוח. כאשר רמות ההיסטמין גבוהות באופן חריג, הוא יכול להחמיר מגוון תסמינים אצל ילדים:
– חרדה, לעיתים עם חרדת נטישה פתאומית.
– OCD, הפרעה טורדנית-כפייתית עם מחשבות חוזרות וטקסים כפייתיים.
– טיקים מוטוריים וקוליים.
– היפראקטיביות דמוית ADHD, עם קושי בשליטה בדחפים.
הקשר הזה אינו תיאורטי בלבד. מחקרים כמו זה של Haas & Panula (2003) מראים כי ההיסטמין מיוצר בגרעין הטוברומממילרי בהיפותלמוס ומשפיע על עוררות, שינה ורגשות דרך ארבעה סוגי רצפטורים (H1-H4). עודף היסטמין מפעיל רצפטורים אלה ביתר, מה שגורם לגירוי יתר עצבי ומגביר תסמינים נוירולוגיים.
מקורות להסטמין: חיידקי המעיים
בניגוד לתפיסה הרווחת, עודף היסטמין אינו נובע רק ממזונות עשירים בהיסטמין. לעיתים קרובות, המקורות העיקריים הם פנימיים ובלתי צפויים.
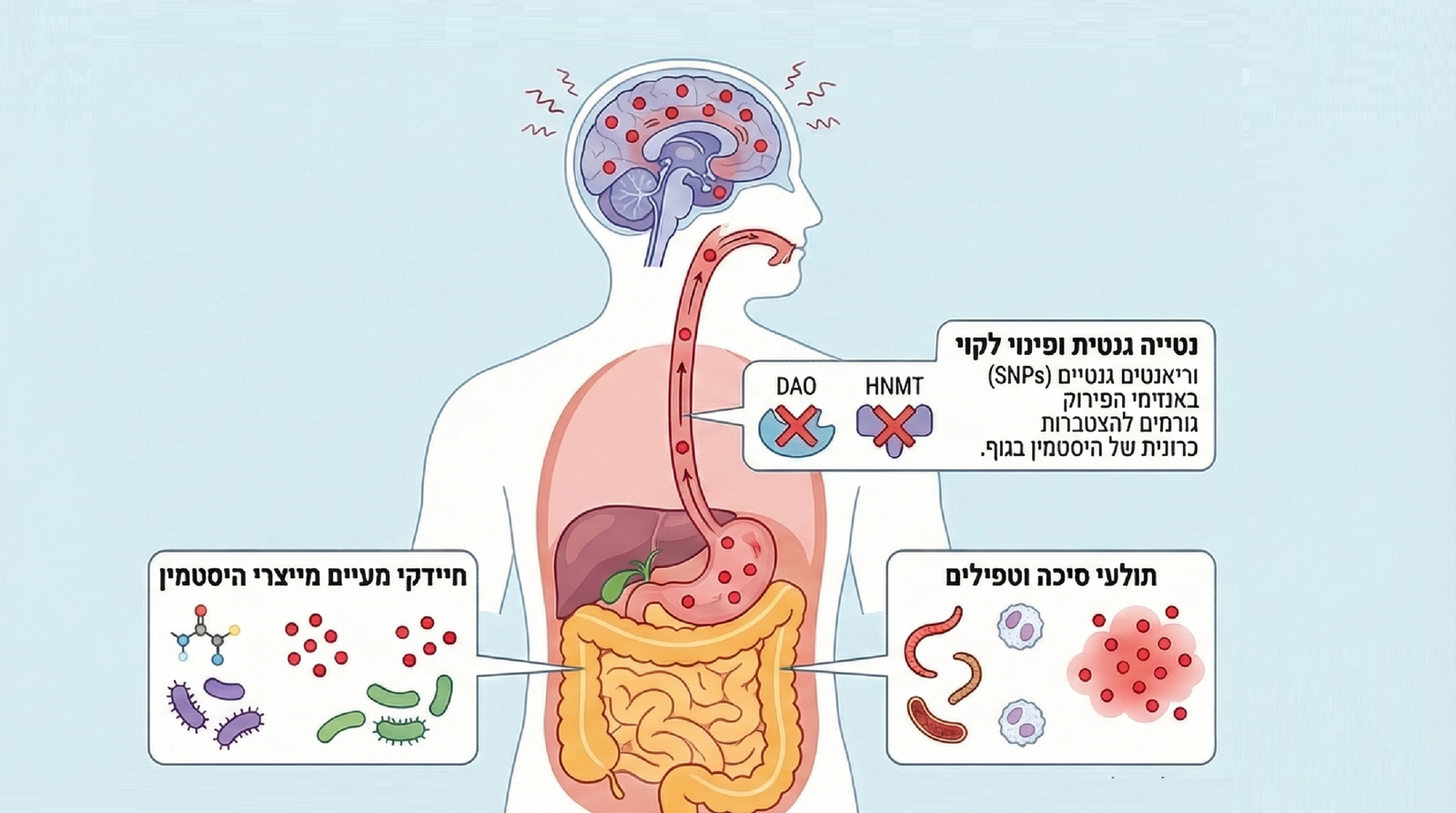
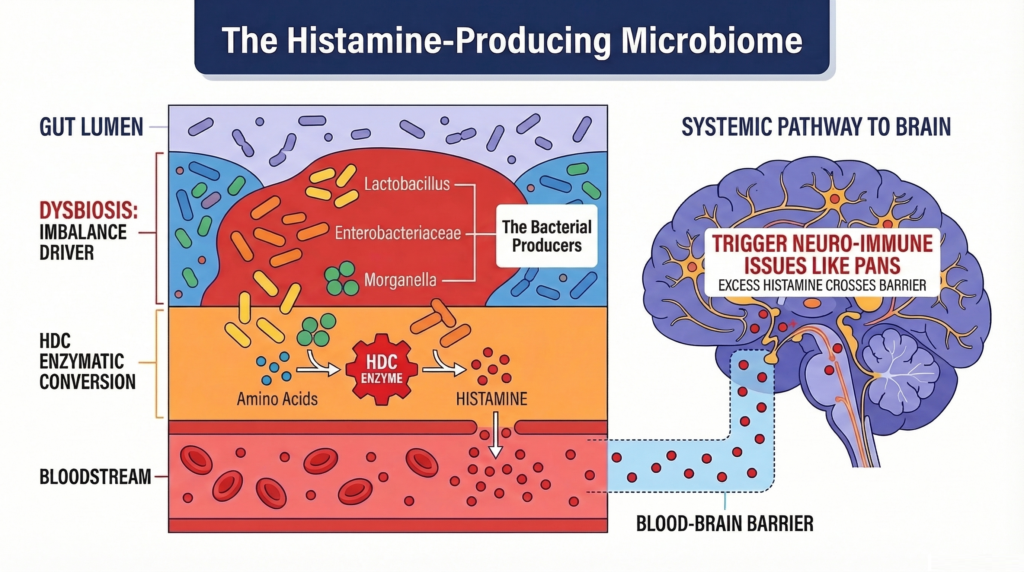
חיידקים מסוימים במערכת העיכול הם “יצרני היסטמין פוריים” שיכולים לגביר את כמות ההיסטמין בגוף. חיידקים כמו Lactobacillus, Enterobacteriaceae ו-Morganella ממירים חומצות אמינו להיסטמין ישירות במעי. כאשר הם בשגשוג יתר (דיסביוזיס), הם מייצרים כמויות גדולות שחודרות למחזור הדם, ולאנשים עם מחסום מוח דליף, חודר ההסטמין למוח. מחקר של Grijsven et al. (2025) מדגיש את תפקיד הדיסביוזיס בהפרעות נוירו-חיסוניות כמו PANS.
דיסביוזיס נפוץ אצל ילדים עם תסמינים נוירולוגיים, שכן חיידקים אלה מייצרי היסטמין בכמות גדולה יחסית.
היסטמין טיקים, תולעים ואלרגניים נוספים
מקורות נוספים כוללים תולעים (threadworms) ואלרגנים סביבתיים. טריגרים אלה גורמים לדה-גרנולציה של תאי מאסט (mast cells) ואאוזינופילים – תאי חיסון שמשחררים היסטמין מאוחסן. Schneider et al. (2006) מראים כי ציר cAMP-אאוזינופילים מגביר שחרור זה, מה שמוביל ל”סופת היסטמין” במחזור הדם שחוצה את מחסום הדם-מוח. אצל ילדים רגישים, תהליך זה מחמיר תסמינים כמו טיקים וחרדה, כפי שמתואר במחקר של Zhang et al (2020).
היסטמין והקשר האנזימטי
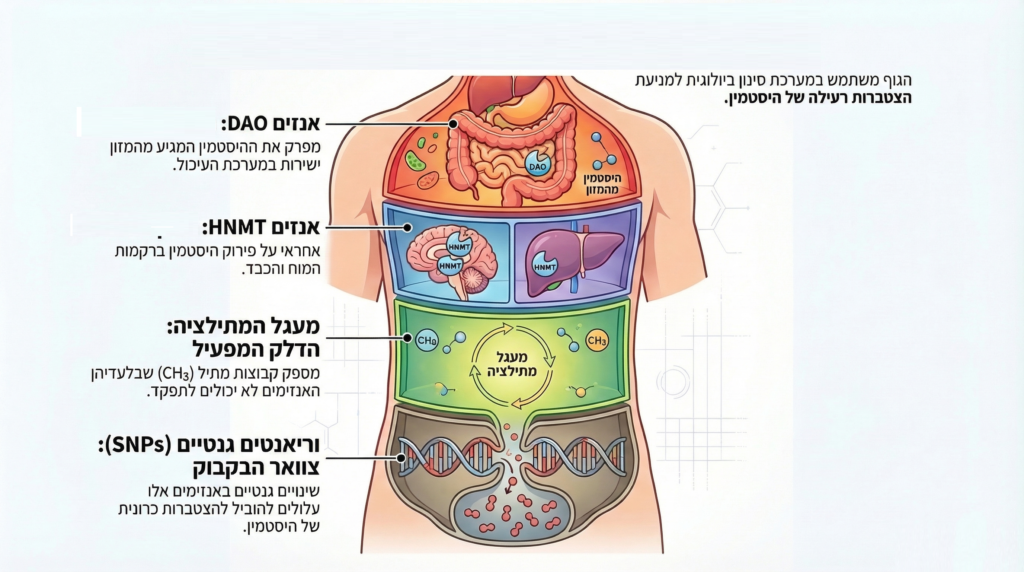
הגוף מפרק היסטמין בעיקר באמצעות שני אנזימים: DAO (diamine oxidase) במעיים ו-
HNMT (histamine N-methyltransferase) במוח ובכבד. ילדים עם פרופיל ביולוגי מסוים כפי שמתאר Hagmeyer (2025), מתקשים בפינוי היסטמין. מה שמוביל להצטברות כרונית.
Sánchez-Pérez et al. (2020) מסכמים כי intolerance להיסטמין הוא לעיתים גנטי, ומשפיע על 1-3% מהאוכלוסייה.
היסטמין ו ADHD
Brighten (2025) בוחן את תפקיד ההיסטמין ב-ADHD, ומראה כי עודף של H3 receptors מגביר היפראקטיביות. Rapanelli et al. (2017) מראים כי הפעלת H3R מפחיתה היפר-תנועתיות, מה שמצביע על פוטנציאל טיפולי. Tuomisto & Tuomisto (1980) הניחו את היסודות להבנת ההיסטמין במוח.
אסטרטגיות עקרוניות לטיפול
- תמיכה במיקרוביום: בדיקות מיקרוביום מאפשרות לזהות את מגוון חיידקי המעיים. בדיקות אלה מאפשרות לבחון האם חיידקים מסויימים המייצרים היסטמין נמצאים בכמות משמעותית. במידה וכן, עיקר הטיפול יהיה לאזן את חיידקי המעי כך שכמות החיידקים הכוללת תהיה מאוזנת.
- תמיכה במסלולים ביולוגיים המשפיעים על פרוק היסטמין ופינוי הסטמין. האם נדרשת תמיכה ל”צוותי פרוק ופינוי”?
- מייצבי מאסט: מדובר בחומרים שונים בין אם כתוספים ובין אם בצמחי מרפא אשר מאפשרים לווסת את התגובה החיסונית. כאשר המידע הנכון נמצא : מי הם בדיוק “השחקנים” הלוקים בתפקידם: חיידקים / אנזימים / מסלולים, ניתן להתאים את הטיפול המתאים.
- תזונה low-histamine תפריט דל בהיסטמין עשוי לתרום לירידה בכמות ההסטמין הקיימת בגוף בתקופת זמן נתונה.
מחשבה לסיום
ניהול תסמינים כמו טיקים, חרדה וOCD דורש מאיתנו לעיתים להסתכל מעבר לברור מאליו. ההבנה שמקור הבעיה עשוי להיות בחיידקי המעיים, במסלולים ביולוגים או בסביבה, פותחת דלת לפתרונות ממוקדים ויעילים יותר.
מאמר זה נועד למטרות לימודיות בלבד ואינה מהווה ייעוץ רפואי פרטני. חשוב לפנות לייעוץ של איש מקצוע כדי להעריך מהו הטיפול הנכון עבור ילדכם. אם יש לכם שאלות, שוחחו עם רופא המשפחה שלכם או תאמו שיחת ייעוץ ללא עלות, שבה נוכל לדון בנסיבות האישיות של משפחתכם.
Brighten, J. (2025). The role of histamine in ADHD
Ercan, A., et al. (2022). Commonly prescribed antihistamine is linked with elevated rates of tic, anxiety and conduct disorders. BC Children’s Hospital Research Institute.
Grijsven, L. J., et al. (2025). Histamine-producing intestinal dysbiosis and its role in neuroimmune disorders. PMC, PMC12787463.
Haas, H. L., & Panula, P. (2003). The role of histamine and the tuberomammillary nucleus in the nervous system. Nature Reviews Neuroscience, 4(3), 121–130.
Hagmeyer, D. (2025). Is histamine intolerance genetic? Understanding DAO & HNMT enzyme SNPs.
Rapanelli, M., et al. (2017). Histamine H3R receptor activation in the dorsal striatum dampens methamphetamine-induced hyperlocomotion. Translational Psychiatry, 7(2), e1027.
Sánchez-Pérez, S., et al. (2020). Histamine intolerance: The current state of the art. BioEssays, 42(10), e2000064.
Schneider, E., et al. (2006). Histamine modulates mast cell degranulation through an up-stream cAMP-eosinophil axis. European Journal of Immunology, 36(2), 408–417.
Tuomisto, L., & Tuomisto, J. (1980). Histamine in the brain. Medical Biology, 58(4), 227–235 PMC6558030).
Zhang, X., et al. (2020). Targeting presynaptic H3 heteroreceptor in nucleus accumbent to improve anxiety and OCD-like behaviors. Proceedings of the National Academy of Sciences, 117(51), 32651–32658.