מחקר PANS PANDAS 2025: המהפכה הגנטית-אימונולוגית
מחקר PANS PANDAS 2025 שפורסם לאחרונה על ידי Prof. Russell C. Dale (2025) וצוותו, חושף ממצאים המשנים את מה שידענו על התסמונת. העבודה המדעי המרתקת הזו עונה על השאלה : מדוע ילד אחד מפתח טיקים, OCD או חרדה אחרי מחלה פשוטה, בזמן שאחיו נותרים בריאים? האם ייתכן שהגנטיקה, ולא רק הזיהום החיצוני, היא הגורם המכריע שקובע אם PANS יופיע? וכיצד טיפול ב-IVIG מצליח לבצע “איפוס אפיגנטי” למערכת החיסון? מאמר זה מנגיש את עיקרי הממצאים בנושא דיסרגולציה אימונית ואפיגנטית כפי שהוצגו ב Webinar: Scientific Research Investigating The Roles of Neuroimmune and Epigenetic Factors, 2025
כמה מילות הקדמה על המחקר
תסמונת PANS PANDAS מהווה את אחת החזיתות המרתקות והמאתגרות ביותר בנוירו-אימונולוגיה בת זמננו. מדובר בהפרעה המערערת את עולמו של הילד ומשפחתו בבת אחת.
במשך שנים רבות, הקהילה המדעית התמקדה בחיפוש אחר ה”טריגר” החיצוני: חיידק הסטרפטוקוקוס במקרה של PANDAS או גורמים זיהומיים וסביבתיים אחרים במקרה של PANS. אולם, עבודתו של Prof. Russell C. Dale וצוותו מסיטה את מרכז הכובד של הדיון המדעי מהגורם החיצוני אל המארח.
מאמר זה סוקר את עבודת המחקר כפי שפורסמה והוצגה בדצמבר 2025. המאמר מציג את הקשר בין המטען הגנטי לבין מערכת החיסון, ויסביר כיצד הנטייה הגנטית עשויה להוביל לדלקת מוחית ולתסמינים נוירו-פסיכיאטריים סוערים.
גודל המדגם ושיטות המחקר:
– קבוצת ה-NDD הכוללת: 100 ילדים (מתוכם 32 עם PANS ו-68 עם הפרעות נוירו-התפתחותיות אחרות).
– קבוצת ביקורת: 58 ילדים עם התפתחות תקינה.
הנטייה הגנטית כגורם שורש
קביעתו של Prof. Russell C. Dale וצוותו כי תסמונת PANS PANDAS נובעת מנטייה גנטית מציבה תשתית תיאורטית המסבירה מדוע רק אחוז קטן מהילדים הנחשפים לזיהומים מפתח תסמינים.
לדבריו, הגנטיקה היא משפיעה על האופן כיצד המערכת תגיב למצבי עקה.
בהתבסס על הנחת היסוד של Prof. Russell C. Dale וחוקריו, ניתן להעריך כי המנגנונים הגנטיים המעורבים כוללים מספר צירים מרכזיים:
- מערכת ה HLA (“Human Leukocyte Antigen”) – זהו הציר המרכזי שבו הגנטיקה פוגשת את האימונולוגיה. וריאנטים גנטיים במערכת ה-HLA משפיעים על האופן שבו תאי מערכת החיסון מזהים אנטיגנים זרים מול אנטיגנים עצמיים. נטייה גנטית בתחום זה עלולה להוביל לזיהוי שגוי של רקמת מוח כגורם עוין.
- מסלולי ה-MBL (“Mannose-binding lectin”) – גנטיקה המשפיעה על מערכת החיסון המולדת ועל היכולת לפנות פתוגנים ביעילות. פגמים גנטיים בייצור חלבונים אלו יוצרים תגובה דלקתית לא מבוקרת.
- ויסות ציטוקינים ורגישות התא – המטען הגנטי קובע את סף הרגישות של רצפטורים לציטוקינים פרו-דלקתיים. אצל ילדים עם נטייה מוקדמת, המערכת עלולה להיכנס ל”סופת ציטוקינים” מקומית שקשה לכבותה.
הגנטיקה, אם כן, אינה רק גורם סיכון, אלא היא “לוח התשתית” שעליו נבנה הסיפור הקליני. ללא הנטייה המוקדמת עליה הצביעו Prof. Russell C. Dale וצוותו, סביר להניח שהזיהום היה מסתיים בתחלואה שגרתית ולא בהתפרצות נוירו-פסיכיאטרית.
המנגנון החיסוני והקשר שלו למטען הגנטי
בניית המודל הנוירו-אימונולוגי המודרני, הנשען על תפיסת הנטייה הגנטית של Prof. Russell C. Dale וחוקריו, חושפת תהליך רב-שלבי שבו הגנים מכתיבים תגובה חיסונית לקויה.
אצל ילדים בעלי נטייה כזו, מערכת החיסון מגיבה בצורה לא טיפוסית לגירויים.
התהליך המרכזי מכונה “חיקוי מולקולרי” (Molecular Mimicry). בשל דמיון מבני בין חלבוני הפתוגן לחלבוני הגוף, ובשל כשל גנטי במנגנוני הסבילות החיסונית, נוצרים נוגדנים עצמיים (Autoantibodies).
אחד ההיבטים הקריטיים שהנטייה הגנטית משפיעה עליהם הוא שלמותו של מחסום הדם-מוח (-Blood-Brain Barrier).
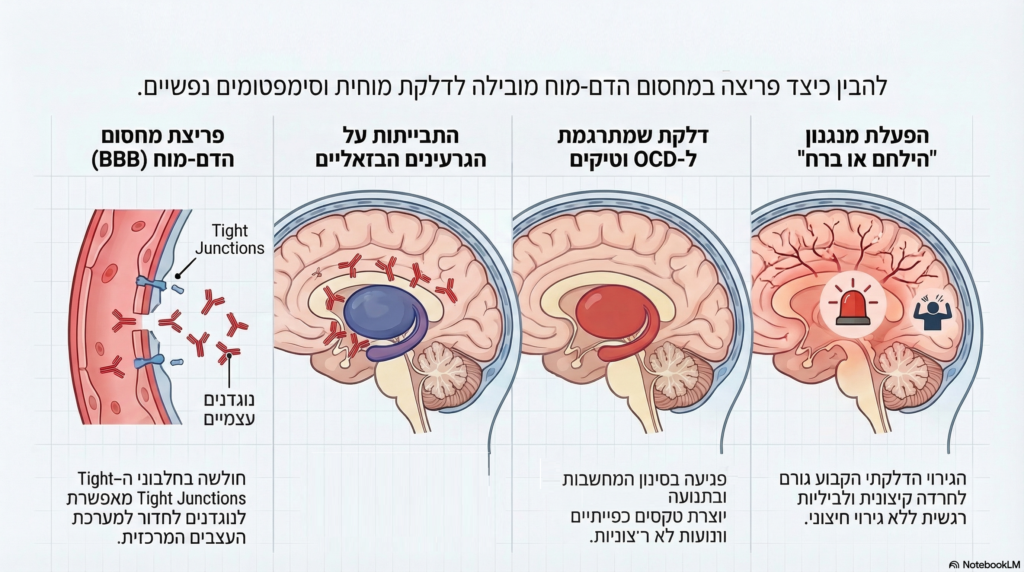
במצב תקין, מחסום הדם-מוח מונע חדירת נוגדנים ותאי דלקת למוח.
אצל ילדים עם PANS PANDAS, קיימת סברה כי קיימת חולשה גנטית בייצור חלבוני ה-Tight Junctions המרכיבים את המחסום.
כאשר מחסום זה נפרץ, נוגדנים עצמיים חודרים למערכת העצבים המרכזית ומתבייתים על הגרעינים הבזאליים (המכונים גם “קשרי בסיס”). אזור זה במוח אחראי על בקרת התנועה, וויסות רגשי וסינון של מחשבות ודחפים.
הדלקת בגרעינים הבזאליים מתרגמת באופן מיידי לסימפטומים הקליניים:
הפרעה טורדנית-כפייתית (OCD) — פגיעה בסינון המחשבות מובילה למחשבות טורדניות וטקסים כפייתיים.
טיקים מוטוריים וקוליים — חוסר יכולת של הגרעינים הבזאליים לדכא תנועות לא רצוניות.
חרדה קיצונית ולביליות רגשית — תגובת “הילחם או ברח” שמופעלת ללא גירוי חיצוני הולם בשל הגירוי הדלקתי הקבוע.
המנגנון האפיגנטי: גנטיקה איננה גזירת גורל והשפעת טיפול IVIG
אם נחשוב על הגנטיקה של הילד כעל “תוכנית בסיסית”, האפיגנטיקה היא הכוח שמחליט אילו חלקים בה יופעלו. זהו התחום החוקר כיצד גורמים סביבתיים וביולוגיים משפיעים על פעילות הגנים, מבלי לשנות את רצף ה-DNA עצמו.
במחקר נבדקה השפעת IVIG על הביטוי הגנטי: הממצא המרכזי הוא שהטיפול ב-IVIG פועל כסוג של “איפוס” למערכת החיסון. לאחר העירוי, נצפתה עלייה משמעותית ביכולת של תאי הדם הלבנים להגיב לזיהומים. במילים אחרות, ה-IVIG עוזר לשחרר את “החסימה” הגנטית ולאפשר למערכת החיסון לחזור לתפקוד תקין ומאוזן יותר.
עם זאת, למחקר יש מספר מגבלות משמעותיות שחשוב לקחת בחשבון:
ראשית, המדגם היה קטן מאוד, וחלק גדול מהם אובחנו גם עם אוטיזם, מה שמקשה לקבוע אם הממצאים ייחודיים רק ל-PANS.
שנית, הטיפול ב-IVIG לא הביא לריפוי מלא; אף ילד לא הגיע לשיפור של 100%, וההטבה הקלינית הייתה לרוב זמנית (נמשכה 2-3 שבועות), מה שמצריך עירויים חוזרים.
בנוסף, המחקר בדק תאי דם ולא תאי מוח, ולכן הקשר הישיר בין השינויים בדם לבין התסמינים הנוירולוגיים עדיין דורש הוכחה נוספת במחקרים נרחבים יותר.
במילים אחרות, האפיגנטיקה היא הגשר המתווך בין הפוטנציאל התורשתי לבין המציאות הרפואית בשטח. הבנה זו מעניקה לנו פתח של תקווה: גם אם קיימת נטייה מולדת, ישנה אפשרות להשפיע על אופן הביטוי שלה, ובכך “לווסת” את עוצמת התסמונת ולפתוח דלת לדרכי התערבות וטיפול חדשות.
כתבה זו היא חלק מסדרת מאמרים העוסקת בכל הקשור ל PANS ו PANDAS.
סדרה זו נועדה למטרות לימודיות בלבד ואינה מהווה ייעוץ רפואי פרטני. חשוב לפנות לייעוץ של איש מקצוע כדי להעריך מהו הטיפול הנכון עבור ילדכם. אם יש לכם שאלות, שוחחו עם רופא המשפחה שלכם או תאמו שיחת ייעוץ ללא עלות, שבה נוכל לדון בנסיבות האישיות של משפחתכם.
להמשך למידה והעמקה בנתוני המחקר
Epigenetic, ribosomal, and immune dysregulation in pediatric acute-onset neuropsychiatric syndrome
Velda X Han, Sarah Alshammery, Brooke A Keating, Brian S Gloss, Markus J Hofer, Mark E Graham, Nader Aryamanesh, Lee L Marshall, Songyi Yuan, Emma Maple-Brown, Jingya Yan, Sushil Bandodkar, Kavitha Kothur, Hiroya Nishida, Hannah Jones, Erica Tsang, Xianzhong Lau, Ruwani Dissanayake, Iain Perkes, Shekeeb S Mohammad, Fabienne Brilot, Wendy Gold, Shrujna Patel, Russell C Dale.
